Lungcancer
I Sverige insjuknade 2 895 män och kvinnor i lungcancer år 1999. Incidens per 100 000 invånare: 34,1 för män och 21,7 för kvinnor. Sjukdomen fortsätter att öka bland kvinnor medan den bland männen har nått en platå.
Endast en minoritet av patienterna har en liten isolerad tumör vid diagnostillfället
Den största enskilda riskfaktorn för att utveckla lungcancer är tobaksrökning (85-90%).
Andra identifierade (ovanliga) orsaker till lungcancer är bland annat radongas, asbest och tungmetaller.
Se även nationella riktlinjer på www.slmf.se.
Indelning
Skivepitelcancer (35%) – Starkt korrelation till rökning. Växer centralt.
Adenocarcinom (35%) – Minst korrelerad till rökning. Varierande förlopp. Växer oftast perifert.
Småcellig (20%) – Starkt korrelering till rökning. Mycket malign, metastaserar tidigt.
Storcellig (10%) – Liknar kliniskt småcellig cancer men behandlas som icke-småcellig.
Carcinoid (1%) – Paraneoplastiska fenomen. Svara bra på kirurgi (5-årsöverlevnad 70-100%).
Symptom
- Hosta (förändrad, nytillkommen, > 3 veckor)
- Pneumoni (recidiverande/långsam regress)
- Blodiga upphostningar
- Smärtor, thorakala och diffusa
- Heshet (rekurrenspares)
- Stokes krage (vena cava superior-syndrom)
- Avmagring, aptitlöshet och trötthet
- Metastaser (lever, skelett, hjärna, njurar, binjurar)
- Paraneoplastiska syndrom, hyperkalcemi
Utredning
Tumörutredning
- Klinisk undersökning med särskild fokus på auskultation, perkussion, ytl lgl och buk.
- Grundutredning lab inkl Hb, Ca, Alb, Leverstatus.
- Lungröntgen och CT-thorax
- Bronkoskopi
- Bronksköljning – cytologi, odling
- Borstprov – cytologi
- Transbronkiell biopsi – histologi
- Transtorakal finnålspunktion – Om den sitter perifert och ej är åtkomlig för px via bronkoskopi.
- Om pleuravätska föreligger bör thorakocentes eller thorakoskopi utföras.
Operabilitetsbedömning
- Spirometri (FEV1 på minst 0,8-1,0 efter op) med diff-kapacitet.
- EKG och Arbets-EKG
- Ev. Radiospirometri, lungscint.
Metastasutredning
- CT-buk eller Ultraljud-buk
- Ev. Skelettskintigrafi
- Ev. PET-scan
- Ev. CT-skalle
- Ev. Mediastinoskopi (inför ev kirurgi om förstorade lgl på CT-thorax).
Stadieindelning
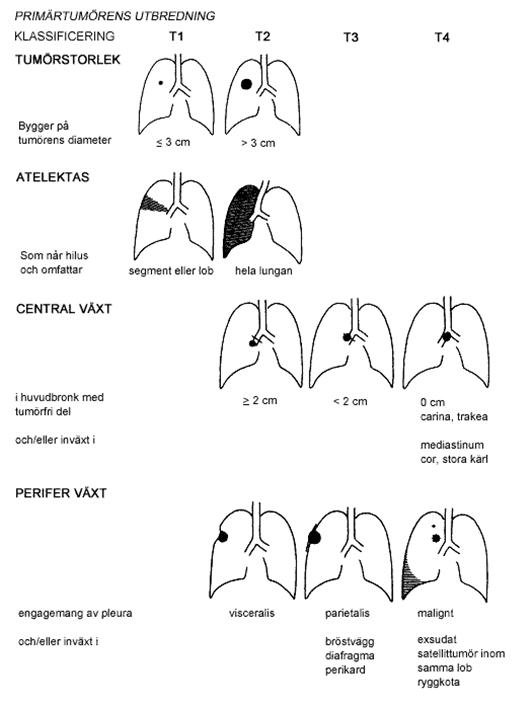
Fynd av regionala lymfkörtelmetastaser N0: inga, N1: ipsilaterala, N2: ipsilaterala inkl carina, N3: kontralaterala mf
MX: metastaser ej bedömt, M0: Inga metastaser, M1, Metastaser
| Stadium | TNM | 5-årsöverlevnad | Behandling (icke småcellig) |
| 0 | Tis, N0, M0 | 100 % | Kirurgi eller strålning |
| IA | T1, N0, M0 | 75 % | Kirurgi eller strålning |
| IB | T2, N0, M0 | 55 % | Kirurgi eller strålning |
| IIA | T1, N1, M0 | 50 % | Kirurgi eller strålning |
| IIB | T2, N1, M0 | 40 % | Kirurgi eller strålning |
| T3, N0, M0 | 40 % | Kirurgi eller strålning | |
| IIIA | T1-3, N2, M0 | 15 % | Kirurgi (?), cyto eller strålning |
| T3, N1, M0 | 35 % | Kirurgi (?), cyto eller strålning | |
| IIIB | T1-3, N3, M0 | 5-10 % | Cytostatika eller strålning |
| T4, N0-3, M0 | 5-10 % | Cytostatika eller strålning | |
| IV | T1-4, N0-3, M1 | 5-10 % | Palliativ cytostatika |
Behandling
Rökstopp. Det har nyligen visats att rökare som drabbas av såväl småcellig- (5-årsöverlevnad 29% vs 63%) som icke-småcellig lungcancer (5-årsöverlevnad 33% vs 70%) i tidigt stadium förbättrar cancerprognosen markant om de slutar röka (2).
Stadieindelning enligt TNM
I-II lokal sjukdom – operabel
III lokoregional sjukdom – ev. operabel
IV fjärrmetasatatisk sjukdom – ej operabel
Endast sammanlagt 20-25% av lungcancerpatienterna kan erbjudas kurativt syftande kirurgi.
Småcelliga lungcancrar är nästan aldrig operabla (p.g.a. av tidig metastasering) dessa (och de inoperabla icke-småcelliga lungcancrarna) behandlas med flera olika cytostatika och strålning mot primärtumör.
Operation
Lobektomi är det minsta kirurgiska ingreppet som görs. Pulmektomi om tumören berör lungans samtliga lober.
Postoperativ 30-dagars mortalitet är idag 3-4% efter pulmektomi och 1-2% efter lobektomi.
Komplikationer inkluderar arytmi (3-30%), hjärtherniering, lobär torsion, luftläckage (drän 1 v), bronkopleural fistel, blödning och kylothorax. Smärta mycket vanlig, 50% har kvar efter 1 år.
Småcellig lungcancer (SCLC)
Begränsad sjukdom defineras som tumörutbredning inom ipsilaterala hemithorax och kan innefattas inom ett tolerabelt strålfält (Stadie IIIA, T3N1M0). Även kontralateral mediastinal och ipsilateral spridning till fossa supraclav brukar innefattas i definitionen begränsad sjukdom (Stadie IIIB, T3N3M0).
Däremot är påvisad pleural (T4) eller perikardcarcinos (T4) defineierade för spridd sjukdom liksom lgl-spridning till kontralaterala fossa supraclav (N3). Spridning till kontralaterala hilus (N3) brukar vanligen hänföras till spridd sjukdom. Således kan Stadie IIIB (T3N3M0) också betyda spridd sjukdom om nu körteln supraclav sitter kontralateralt eller N3-körteln sitter i hilus i stället för i mediastinum.
Primärutredningen innefattar förutom grundutredning även kontrast-DT eller MRT av hjärnan och skelettscint. PET-CT kan övervägas men är ej obligat.
Begränsad sjukdom T1-2N0 dvs Stadium I
Preoperativt görs PET-CT och mediastinoskopi (lungkirurgi är ej motiverat vid påvisande av N1 eller N2-spridning) samt DT eller MRT av huvudet.
Om negativ kringutredning inkl mediastinoskopi utförs lobektomi med lgl-utrymning.
Om diagnosen SCLC bekräftas i op-PAD ges adjuvant terapi enl följande:
- Inga påvisade lgl-metastaser: 4 kurer adjuvant cytostatika efterföljt av PCI (profylaktisk cranial irradiation).
- Påvisad N1-spridning individuell bedömning avseende adjuvant kemo eller radioterapi.
Begränsad sjukdom stadium II-IIIB
Vid PS 0-1, ingen terapibegränsande komorbiditet, FEV1>40% av predikerad kan konkomitant platinumbaserad kemoradioterapi med tidigt insatt accelererad hyperfraktionerad thoracal strålbehandling ges. Behandlingen är kurativt syftande.
- Karboplatin eller Cisplatin ges tillsammans med Etoposid (Etopsid, Vepesid) i 4 kurer. Karboplatin ger mindre subjektiva biverkningar och är enklare att administrera. Cisplatin är mindre benmärgstoxiskt men sämre för njurar, öron och nerver.
- Strålbehandling startas dag 22 samtidigt som kur 2. 1,5 Gy ges 2 ggr dagligen med 6 tim intervall totalt 30 fraktioner under 15 dagar (mån-fre under 3 veckor) till slutdos 45 Gy. Ge profylaktiskt Andapsin och Omeprazol. Blodstatus följs. Uppehåll i strålbehandlingen får endast göras på vitalindikation.
- Vid komplett eller god remission ges profylaktisk cerebral strålbehandling. 3-4 veckor måste förflyta efter given avslutande kur 4. Ges i dosen 2 Gy, totalt 15 fraktioner till slutdos 30 Gy (3 veckor).
Patienter som inte bedöms tolerera ovanstående ges sekventionell kemoradioterapi.
- Karboplatin ges tillsammans med Etoposid med cykellängd 21 dagar.
- 2 veckor efter starten av kur 2 gest strålbehandling med 3 Gy i 10-13 fraktioner till slutdos 30-39 Gy.
- 2 veckor efter starten av avslutad strålbehandling ges ytterligare 2 kurer karboplatin och Etoposid.
- Profylaktisk cerebral strålbehandling skall erbjudas vid komplett eller god remission.
Spridd sjukdom
Irinotecan (Campto) ges tillsammans med Carboplatin i 4 kurer. Campto ger diarré. Atropin skall ges sc innan administration och pat skall förses med Loperamid.
Alternativt kan Carboplatin ges tillsammans med Etoposid i 4 kurer (något sämre resultat).
Profylaktisk cerebral irradiation bör erbjudas till alla med respons på given kemoterapi (såväl komplett som partiell respons). Dock ej vid multipla komorbiditeter, PS 3-4 och nedsatt mental funktion. 2,5 Gy ger i 10 fraktioner till slutdos 25 Gy (2 veckor).
Palliativ strålbehandling kan bli aktuellt vid lokalsymptom.
Tumregel ang cytostatika och progress eller recidiv (1)
- Om progress under behandling, avsluta behandlingen!
- Om det gått > 3 mån men god effekt av tidigare behandling kan man försöka samma behandling igen.
- Om < 3 mån gått sedan sista cytostatikakuren och progress (eller recidiv) av sjukdom bör man byta cytostatikaregim.
Andra linjens behandling
Vid recidiv efter första linjen är behandlingsmöjligheterna begränsade. Medianöverlevnaden ligger på 4-5 mån. Förutsättningarna för 2:a linjens cytostatika är behanlingsmotiverad patient och PS 0-2.
- Vid återfall < 3 mån bör behandlingen inriktas på palliation. I exceptionella fall med yngre behandlingsmotiverad patient kan Amrubicin övervägas.
- Vid återfall 3-6 mån efter senaste givna cytostatikadosen kan Topotecan (Hycamtin) ges. Cykellängd 21 dagar, max 4 kurer.
- Vid återfall > 6 mån reinduceras primärregimen.
- Ett alternativ är Gemcitabine + Paclitaxel (8 dagar).
Best supportive care inkl palliativ strålbehandling bör erbjudas i övriga fall (PS3).
Prognos
| Spridd sjukdom | Begränsad sjukdom | |
| Respons kemoterapi | 60-80% | 70-90% |
| Medianöverlevnad | 9-11 mån | 16-23 mån |
| 2-årsöverlevnad | 5-10% | c:a 40% |
| 5-årsöverlevnad | 3-4% | 10-25% |
Icke småcellig lungcancer
Stadium I, II och IIIA
Operation om patienten är funktionsmässigt operabel.
Extern konventionell strålbehandling alt. precisionsstrålbehandling om patienten ej är funktionsmässigt operabel
Finns idag indikationer, men inte tillräckligt stöd för att regelmässigt ge adjuvant eller neoadjuvant behandling.
Stadium IIIB
Kurativ strålbehandling kan bli aktuellt vid avsaknad av pleuracarcinos eller omfattande tumörbörda som utesluter radioterapi av toxicitetsskäl.
Stadium IIIB (pleuracarcinos och stor tumörbörda) och VI
Cytostatikabehandling palliativ om pat bedöms tåla detta. Performace-status på 0-2 är gränsen för CS, nyttan är störst i PS 0-1. Patienten skall vara fullständigt informerad om behandlingsnyttan och mo
Vid pleuraexudat bör pleurodes (5 g talk upplöst i 100 ml NaCl) erbjudas.
Strålbehandling får EJ ges samtidigt som cytostatika (ffa Gemcitabine).
- Thoracal strålbehandling kan starta 1-2 veckor (min 1 vecka) efter senaste Gemcitabine-dosen. Kan återupptas efter min 2 veckor.
- Extrathoracal strålbehandling kan starta 1 vecka (min 3 dagar) efter senaste Gemcitabinedosen. Kan återupptas efter 1 vecka (min 3 dagar).
Laserbehandling, brachyterapi och stentning kan ha en god palliativ effekt.
Komplikationer
Lokala
Endobronkiell tumörväxt (strålning 36 Gy / 12 fraktioner, YAG-laser, stent)
Recurrenspares (lokala operationer, injektioner via ÖNH alt trakeotomi om stora problem).
Phrenicuspares
Vena cava superior-syndrom (palliativ strålning 36 Gy / 12 fraktioner, stent)
Hemoptys (palliativ strålning brukar bita)
Horners syndrom
Revbenserosion
Perikardit
Förmaksflimmer
Metastatiska
Hjärna (strålning 30 Gy / 10 fraktioner alt 20 Gy / 5 fraktioner)
Skelett (smärta, anemi, högt Ca, behandling med strålning engångs 8 Gy)
Lever (hepatomegali)
Binjurar (addisons, kortisontillskott)
Endokrina
ADH (SIADH, lågt Na)
ACTH (Cushings)
PTH (högt Ca)
Icke-metastatiska neurlogiska
Konfusion
Kramper
Cerebellära symptom
Proximal myopati
Perifer neuropati
Polymyosit
Eaton-Lambert syndrom (Myasteniskt syndrom)
Övriga
Klubbning
Dermatomyosit
Acanthosis nigricans
Trombophlebitis migrans
Referenser
- Löfvenberg J, Undervisning, G. Norrman, Editor. 2007: Östersund.
- Rökstopp förbättrar lungcancerprognosen. Läkartidningen nr 9 2010 Vol 107.