Tillväxthormonbrist
Symptom
Kommer tidigt i hypofysära sjukdomsförlopp men är svårdiagnostiserad. GH-bristen är svår att upptäcka både för patienten och läkaren.
Ökad fettansamling, minskad muskelmassa, tunn krackelerad hud.
Okarakteristiskt nedsatt livskvalitet med trötthet, uttröttbarhet, dålig sömn såväl som dålig vakenhetsperiod. Låg energinivå, depressivitet, nedsatt initiativ- och koncentrationsförmåga och låg livskvalitet.
Utredning
Utredning avseende GH-brist kan utföras vid misstanke om brist och där påvisad brist föranleder substitution i följande situationer (2):
- Sjukdom i hypotalamus/hypofys.
- Strålning mot hjärnan (ITT är bäst, GHRH-Argnintest undersöker inte hypotalamus funktion).
- Traumatisk hjärnskada (vänta 1 år innan utvärdering görs, övergående brist är inte ovanligt (2)).
Primär GH-brist som en isolerad entitet erkäns inte som egen sjukdom.
Diagnos
GH-brist kan inte fastställas med enstaka GH-analyser.
Insulin-like growth factor-1 (IGF-1), som speglar tillväxthormonsöndringen över dygnet, är inte heller diagnostiskt för GH-brist hos vare sig barn eller vuxna. Provet är mest tillförlitligt vid ålder < 40 år och BMI < 25 (2). Ett för åldern lågt IGF-1-värde vid förekomst av sjukdom i hypofysen talar starkt för GH-brist, men ett normalt IGF-1 utesluter inte GH-brist.
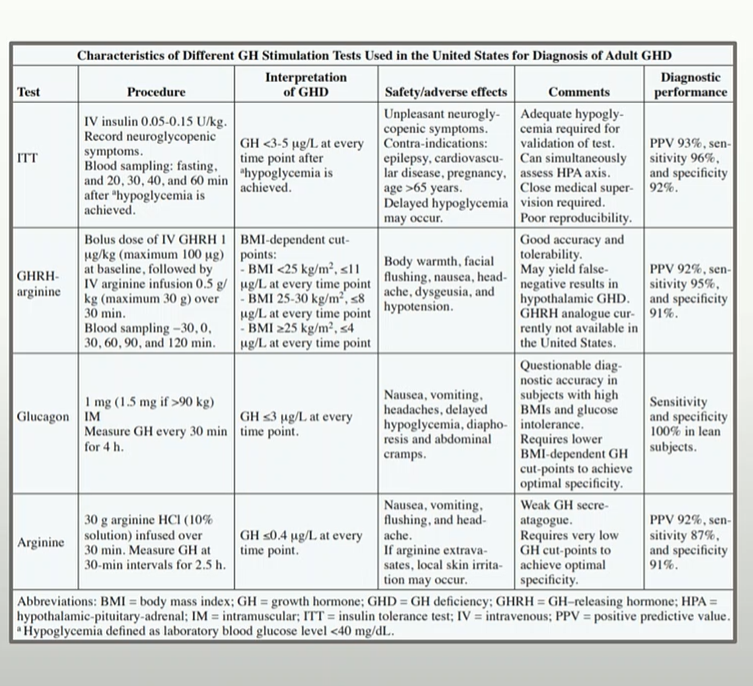
För en säker/säkrare diagnos krävs stimuleringstester. Bakgrunden är att interventionen stimulerar frisättningen av GH och uteblivet adekvat svar indikerar brist. Ett stiumleringstest är tillräckligt för diagnostisering av adult GHD (2). De som är bäst validerade och rekommenderas enl konsensus (2) är
- Insulininducerad hypoglykemi (ITT) (kan också identifiera sviktande ACTH-produktion, anses vara bäst efter strålbehandling då de kombinerade stimuleringstesten stimulerar både hypofys och hypotalamus).
- GHRH + Arginin-stimuleringstestet
- Glukagon-stimuleringstestet
- GHRH + GHRP-stimuleringstestet
- Argininstimulering kan bara användas men bara vid BMI < 25 (2).
Vid organisk hypofyssjukdom med samtidig svikt av tre ller fyra hypofysaxler är sannolikheten för GH-brist 95-97% (2). I sådana fall behöver inte stimuleringstest utföras för diagnos (2).
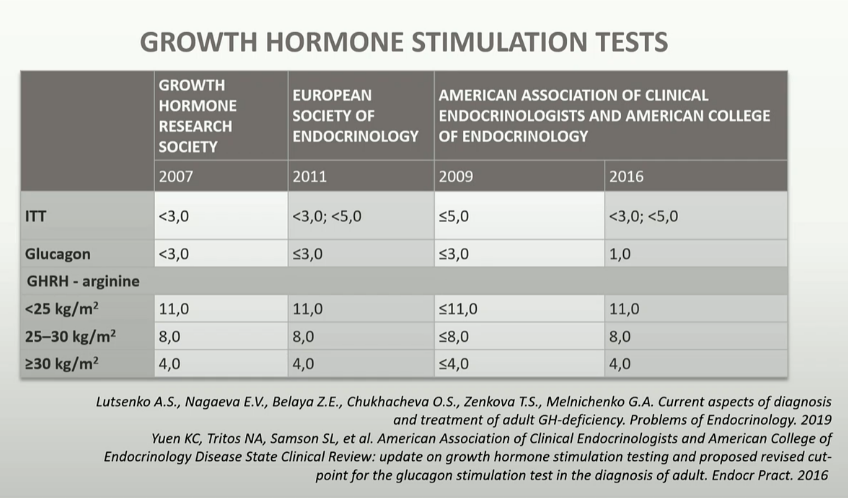
Vid provokationstest minskar sannolikheten för uttalad GH-brist i takt med ökande STH-max över 3 µg/L. STH-max påverkas starkt av individens nutritionssituation. Obesitas medför regelmässigt en så uttalad minskning av blodets STH-nivåer att situationen inte går att skilja från den vid genuin GH-brist. Detta gäller både vid provokationstester och vid mätning av spontansekretion. Fasta (mer än ett dygn) ger däremot en avsevärd ökning både av spontan och provocerad GH-sekretion.
Den gräns som kan motivera GH behandling hos patienter där auxologiska och radiologiska fynd stödjer den kliniska misstanken på STH-brist, är en maximal STH-nivå vid provokationstest <10 ug/L (<24 mU/L, 22kD, WHO IRP 80/505). Något säkert vetenskapligt stöd för denna traditionellt använda nivå finns emellertid inte.
Behandling
Indikationen för behandling är svår. Vid ålder > 70 år initieras mycket sällan behandling. Vid ålder 60-70 hamnar man i gränslandet men vid ålder < 60 år bör man ha lågt i tak för att utreda/behandla.
I transitionsåldern (efter full längd, vanligen före 20-års ålder) skall behovet av GH-behandling på nytt utvärderas och ställningstagande till fortsatt behandling tas hos de patienter med GH-brist i barndomen. Vid transkriptionsfaktormutation (POU1F1, Pit-1, PROP-1, HESX-1, LHX-3, LHX-4), mer än tre sviktande axlar och vid isolerad GH-brist pga mutation (GH-1, GHRH-R) behöver inte indikationen omvärderas (2). I övriga fall sätts GH-behandlingen ut och förnyad testning görs efter minst 1 mån. Om IGF-1 indikerar brist kan detta räcka, annars görs GHRH-arginin eller ITT för att skärpa diagnostiken.
När GH-behandling gjorts utan påvisad GH-brist (Turner, SGA) finns ingen indikation för GH-behandling i vuxen ålder. En GH-peak < 6 ug/l vid ITT i tranistionsperioden indikerar kvarvarande GH-brist (2). Förnyad bedömning efter avslutande av somatisk tillväxt (25 års ålder) kan övervägas vid isolerad GH-brist i barndomen (2).
Rekombinant GH i dagliga subkutana injektioner. Dosen, initialt mycket låg hos vuxna (0,1-0,3 mg dagligen) för att undvika besvärande vätskeretention, höjs successivt tills IGF-1 ligger inom normalområdet. Unga kvinnor behöver oftast en högre dos (startdos 0,3 mg/dag (2)) än unga män (startdos 0,2 mg/dag (2)). Vanlig underhållsdos hos kvinnor är 0,7-1,1 mg och hos män 0,3-0,6 mg. Hos äldre patienter rekommenderas startdosen 0,1 mg/dag (2). Den subcutana injektionen ges till kvällen för att efterlikna den normala dygnsrytmen.
Billigaste alternativet är Omnitrope i SurePal-pennan.
Vissa patienter upplever ett ökat välbefinnande inom någon månad, andra först efter ett år. Aktiv malign sjukdom är en kontraindikation för GH-behandling men det finns inga belägg fr att GH-behandling ökar risken för tumörrecidiv eller de novo-malignitet (2).
Påverkan på andra hormoner (2)
- Peroral östrogenbehandling minskar GH-effekten.
- Uppstart av GH-behandling kan demaskera sekundär binjurebarksinsufficiens genom reducerad aktivitett av 11B-HSD1. Hydrokortisondosen kan behöva ökas hos de som redan substitueras. Förnyad utredning av HPA-axeln rekommenderas hos de som tidigare inte bedömts ha kortisolsvikt efter start av GH-behandlingen.
- GH ökar perifer konversion av T4 till T3. GH-behandling kan demaskera central hypotyreos genom att T4 efter behandling sjunker under subnormal nivå. Vid levaxinbehandling kan dosen behöva ökas.
Uppföljning
Behandlingseffekten följs kliniskt samt genom mätning av biokemi och kroppskonstitution.
IGF-1 skall mätas minst årligen. Efter dosjustering kan utvärderande provtagning göras tidigast 6 veckor senare. IGF-1 skall hållas under övre normalområdet (ålder och vikt-korrigerat) oavsett utgångsnivå (2).
DEXA för värdering av skelettet rekommenderas vid baseline samt vartannat år därefter eftersom skelettmineraliseringen kan minska genom ökad remodellering (2).
Patienter med ökar risk för typ 2-diabetes skall följas noggrannt då GH-behandling kan minska insulinkänsligheten (2). Uppkomst av diabetes behandlas på sedvanligt sätt.
Referenser
- Werner S: Endokrinologi. 2 ed. Liber, Ljubljana, 2007.
- Ho K et al: Consensus guidelines for the diagnosis and treatment of adults with GH deficiency II: a statement of the GH Research Society in association with the European Society fo Pedriatic Endocrinology, Lawson Wilkins Society, European Society of Endocrinology, Japan Endocrine society and Endocrine Society of Austrlia. European Journal of Endocrinology (2007) 157, 695-700.